Benzol
Entdeckung: 1824 wurde das Benzol durch Michael Faraday entdeckt. Er isolierte das Benzol aus komprimiertem Leuchtgas. Er nannte es zuerst Doppelt-Kohlenwasserstoff und fand heraus, das in einem Benzolmolekül gleich viele Kohlenstoffatome wie Wasserstoffmoleküle vorhanden sind. Die genaue Summenformel wurde 1834 von Eilhard Mitscherlich entdeckt: C6H6 Er gab dem Stoff den Namen Benzin, im gleichen Jahr wurde es aber von Justus Liebig in Benzol umbenannt, wobei es bis heute geblieben ist.
1865 stellte der deutsche Chemiker August Kekulé zum ersten mal die Strukturformel von Benzol auf, nach der die sechs Kohlenstoffatome einen Ring bilden. Einfach- und Doppelbindungen wechseln sich ab. An jedem Kohlenstoffatom hängt noch ein Wasserstoffatom. 1988 ist es Wissenschaftlern zum ersten Mal gelungen, das Benzolmolekül unter einem Raster-Tunnel-Elektronenmikroskop sichtbar zu machen.
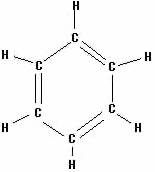
Eigenschaften: Benzol gehört zu den Aromaten und verfügt über folgende wichtige Eigenschaften: flüssig, farblos, leicht beweglich, charakteristischer Geruch, hoher Kohlenstoffanteil, leichtentzündlich, brennt mit stark rußender Flamme, krebserzeugend, giftig bei Berührung mit der Haut und bei Verschlucken/Einatmen, letzteres führt zu Schwindel, Erbrechen, Übelkeit bis hin zur Bewußtlosigkeit, chronische Vergiftungen führen zu Schädigungen des Knochenmarks, der Leber und der Nieren und zu Leukämie
Herstellung: Benzol entsteht hauptsächlich bei der Destillation von Steinkohle und von Erdöl. Bei der Weiterverarbeitung des Erdöls fällt Benzol beim Cracken von Benzin an. Durch Reformieren von Benzin entsteht Superbenzin, bei dem das Benzol dann schon direkt enthalten ist. Beim Reformieren wird der ringförmige Kohlenwasserstoff Cyclohexan zu Benzol dehydriert:
C6H12 C6H6 + 3H2
Verwendung: Benzol wird als wichtiges Lösungsmittel in der chemischen Industrie verwendet. Zudem dient es als Ausgangsstoff für viele organische und aromatische Verbindungen, z.B. Insektizide, Kunststoffe und Kunstharze. Wenn man Benzol verbrennt, entsteht dabei eine hohe Verbrennungswärme. Deshalb, und wegen seiner Eigenschaft, Frühzündungen im Ottomotor ('Klopfen') zu verhindern, wird es als Zusatzstoff im bleifreien Benzin verwendet. Wegen der gesundheitsschädigenden Wirkung von Benzol wird versucht, die Freisetzung von Benzoldämpfen zu verringern. Benzoldämpfe gelangen auf viele Arten in die Luft, in erster Linie durch den Kraftzeugverkehr. Zum Einen gelangt es dort über die Motorabgase direkt in die Luft. Deshalb wurde am 1. September 1995 Super Plus-Benzin mit einem Benzolgehalt von maximal einem Prozent eingeführt. Weitere Maßnahmen sind ein verstärkter Einsatz des geregelten Drei-Wege-Katalysators. Zum Anderen werden beim Betanken selbst Benzol-Dämpfe frei. Dagegen wurden an den Tankstellen sogenannte Saugrüssel eingeführt. Dadurch können beim Tanken bis zu 85 % der freiwerdenden Dämpfe aufgefangen und in den Lagertank zurückgeführt werden. Beim Transport des Benzins von der Raffinerie zur Tankstelle werden ebenfalls Benzoldämpfe frei. Weitere Quellen sind Feuerungsanlagen, Kokereien und Kraftstofflager.
Haupt | Fügen Sie Referat | Kontakt | Impressum | Nutzungsbedingungen
